ЦИРРОЗ ПЕЧЕНИ
Злоупотребление алкоголем приводит к в первую очередь к поражению печени. Одной из наиболее тяжелых форм, часто приводящей к летальному исходу, является цирроз печени.
Основные симптомы и показатели тяжелой формы цирроза печени:
 Трофологическая недостаточность поражает все органы и системы. Потеря в весе от 35 до 40% от массы тела считается фатальной. Истощение белка скелетных мышц и внутренних органов (печени, гастроинтестинального тракта, почек и сердца) обычно развивается пропорционально потере массы тела. Прогрессирующая белковоэнергетическая недостаточность приводит к нарушению функции органов. Снижается сердечный выброс и сократительная способность миокарда. Слабость и атрофия дыхательных мышц приводят к нарушению респираторной функции и снижению мукоцилиарного клиренса. Поражение гастроинтестинального тракта проявляется атрофией слизистой и потерей ворсинок тонкой кишки, приводящих к синдрому мальабсорбции. Характерна панкреатическая и тонкокишечная дисахаридазная недостаточность.
Трофологическая недостаточность поражает все органы и системы. Потеря в весе от 35 до 40% от массы тела считается фатальной. Истощение белка скелетных мышц и внутренних органов (печени, гастроинтестинального тракта, почек и сердца) обычно развивается пропорционально потере массы тела. Прогрессирующая белковоэнергетическая недостаточность приводит к нарушению функции органов. Снижается сердечный выброс и сократительная способность миокарда. Слабость и атрофия дыхательных мышц приводят к нарушению респираторной функции и снижению мукоцилиарного клиренса. Поражение гастроинтестинального тракта проявляется атрофией слизистой и потерей ворсинок тонкой кишки, приводящих к синдрому мальабсорбции. Характерна панкреатическая и тонкокишечная дисахаридазная недостаточность.
К наиболее значительным патологическим изменениям в организме при белково-энергетической недостаточности относится нарушение иммунной функции. Число и функциональная способность Т-лимфоцитов снижаются, нарушаются свойства В-лимфоцитов, гранулоцитов, активности комплемента и анатомического барьера инфекции.
Развитие трофологической недостаточности у пациентов с циррозом печени связано с нарушением метаболизма основных питательных веществ (белков, жиров, углеводов). Снижение синтеза плазменных белков приводит к падению уровня циркулирующих протеинов, что клинически проявляется периферическими отеками и асцитом. Уменьшение синтеза белка в мышцах может осложниться мышечной атрофией. В условиях белковой недостаточности снижается продукция гормонов и ферментов, в частности, ферментов поджелудочной железы; недостаточность микроэлементов и витаминов часто служит причиной развития панкреатита. Панкреатическая мальдигестия, дефицит желчных кислот и снижение синтеза энтерокиназ приводят к развитию синдрома мальабсорбции, нарушение всасывания питательных веществ усугубляет трофологическую недостаточность и значительно ухудшает прогноз.
Развитие энергетической недостаточности у больных циррозом печени связано с уменьшением роли углеводов как источника энергии (2% у больных циррозом печени и 38% у здоровых людей) и увеличением доли жиров (соответственно 86 и 45%). Это происходит вследствие уменьшения образования глюкозы печенью и снижения запасов гликогена. После приема пищи у пациентов с циррозом печени отмечается более быстрая утилизация пищевых углеводов из-за нарушения способности печени к их депонированию, что сопровождается мобилизацией триглицеридов в качестве источника энергии.
 С другой стороны, по мере прогрессирования заболевания увеличиваются энергетические затраты организма в покое. Наиболее ранняя и тяжелая трофологическая недостаточность наблюдается у пациентов с алкогольным циррозом печени. Эндогенное истощение, обусловленное основным заболеванием, усугубляется экзогенным истощением больных, пренебрегающих элементарными диетическими рекомендациями в силу социальной деградации и восполняющих запасы энергии "пустыми" алкогольными калориями при повышенной потребности в питательных веществах, витаминах и микроэлементах. В частности, у лиц, потребляющих более 30% от общего количества калорий в сутки в виде алкоголя, имеется высокий риск развития недостаточности всех питательных веществ.
С другой стороны, по мере прогрессирования заболевания увеличиваются энергетические затраты организма в покое. Наиболее ранняя и тяжелая трофологическая недостаточность наблюдается у пациентов с алкогольным циррозом печени. Эндогенное истощение, обусловленное основным заболеванием, усугубляется экзогенным истощением больных, пренебрегающих элементарными диетическими рекомендациями в силу социальной деградации и восполняющих запасы энергии "пустыми" алкогольными калориями при повышенной потребности в питательных веществах, витаминах и микроэлементах. В частности, у лиц, потребляющих более 30% от общего количества калорий в сутки в виде алкоголя, имеется высокий риск развития недостаточности всех питательных веществ.
Для всех больных алкогольным циррозом печени характерна панкреатическая мальдигестия. Ее развитие может быть обусловлено разными механизмами. Во-первых, снижение синтеза ферментов поджелудочной железы происходит из-за общей нехватки белка в организме. Во-вторых, у больных алкогольным циррозом печени, как правило, имеется хронический алкогольный панкреатит, который приводит к внешнесекреторной недостаточности поджелудочной железы. В-третьих, для больных алкоголизмом характерны гиперацидные состояния, приводящие к "закислению" двенадцатиперстной кишки и инактивации кислотонеустойчивой панкреатической липазы.
Нарушение всасывания питательных веществ у алкоголиков может быть обусловлено не только ферментативной недостаточностью поджелудочной железы, но и изменением гастроинтестинальной моторики в результате прямого токсического влияния алкоголя на стенку кишки и гипоплазией слизистой тонкой кишки при недостаточности фолатов. Хроническое потребление алкоголя снижает кишечную активность дисахаридаз (главным образом, лактазы), в результате чего развивается симптоматическое нарушение толерантности к лактозе, что значительно утяжеляет диарею.
Алкоголизм может служить причиной недостаточности большинства витаминов группы В (тиамин, рибофлавин, пиридоксин, фолаты, ниацин, пантотеновая кислота и биотин), витамина А и витамина С. Кроме того, у больных алкоголизмом часто наблюдается дефицит микроэлементов (цинк, селен и магний).
Недостаточность тиамина может выявляться даже у алкоголиков без признаков недостаточности питания и служить причиной развития синдрома Вернике-Корсакова, бери-бери и полинейропатии. Недостаточность рибофлавина характерна для алкоголиков, в особенности для лиц с осложнениями заболевания, требующими госпитализации. Экспериментальные данные показывают, что недостаточность рибофлавина может приводить к снижению продукции протеинов, амилазы, химотрипсиногена и трипсиногена и играть большую роль в развитии панкреатической недостаточности у больных алкоголизмом. Рибофлавин служит предшественником двух энзимов, участвующих в большом количестве реакций, включая промежуточный метаболизм пиридоксина и фолиевой кислоты. Поэтому недостаточность рибофлавина может служить причиной вторичного дефицита пиридоксина и фолиевой кислоты.
Недостаточность пиридоксина отмечается более чем у 50% алкоголиков, даже без нарушений функции печени и гематологических расстройств. В развитии дефицита играют роль как недостаточное поступление с пищей, так и повышенная деструкция и снижение синтеза витамина.
Широко известно, что у алкоголиков часто выявляется дефицит фолиевой кислоты. Недостаточность фолатов может приводить к развитию гипоплазии слизистой тонкой кишки и снижению интестинальной абсорбции других питательных веществ.
 Недостаточность витамина В12 примерно у 40% пациентов связана с нарушением его всасывания. Причем нарушение всасывания витамина В12 может наблюдаться даже при отсутствии факторов, обусловливающих мальабсорбцию витамина (синдром избыточного роста микроорганизмов и илеальная дисфункция). Дело в том, что разрушение связи витамина В12 со связывающим белком происходит при выбросе трипсина в двенадцатиперстную кишку. При снижении секреции ферментов поджелудочной железы нарушение всасывания кобаламина может быть обусловлено пребыванием его в постоянной связи с гаптокоррином (связывающим белком), а также с нарушением энтерогепатической циркуляции витамина.
Недостаточность витамина В12 примерно у 40% пациентов связана с нарушением его всасывания. Причем нарушение всасывания витамина В12 может наблюдаться даже при отсутствии факторов, обусловливающих мальабсорбцию витамина (синдром избыточного роста микроорганизмов и илеальная дисфункция). Дело в том, что разрушение связи витамина В12 со связывающим белком происходит при выбросе трипсина в двенадцатиперстную кишку. При снижении секреции ферментов поджелудочной железы нарушение всасывания кобаламина может быть обусловлено пребыванием его в постоянной связи с гаптокоррином (связывающим белком), а также с нарушением энтерогепатической циркуляции витамина.
Панкреатическая мальдигестия ведет за собой нарушение всасывания жирорастворимых витаминов А, Е, К и D. Дефицит витамина К ухудшает состояние свертывающей системы организма, нарушение деятельности которой характерно для цирроза печени. Недостаточность других жирорастворимых витаминов также способствует нарастанию трофологических расстройств.
У алкоголиков очень часто выявляется недостаточность микроэлементов. Низкий уровень цинка у хронических алкоголиков обусловлен как уменьшением его потребления, так и нарушенным всасыванием и повышенным выделением цинка с мочой. Особенно выражен дефицит цинка у больных циррозом печени. В эксперименте недостаточность цинка вызывает повреждение ацинарных клеток поджелудочной железы и ингибирует синтез панкреатического протеина. В условиях дефицита цинка подавляется гормональная стимуляция секреции бикарбонатов и протеинов. Этот эффект может значительно потенцировать сопутствующая недостаточность липидов. На экспериментальных моделях показано, что недостаточность селена вызывает панкреатическую дегенерацию и фиброз. Низкий уровень селена может также способствовать повреждению ткани поджелудочной железы свободными радикалами. Таким образом, дефицит цинка и селена играют большую роль в развитии как алкогольного, так и трофического панкреатита.
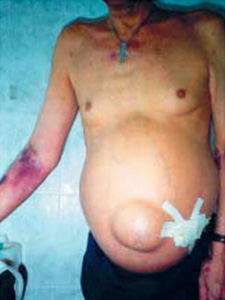
Клинические проявления цирроза печени разнообразны и во многом обусловлены трофологической недостаточностью. К наиболее частым симптомам относятся слабость, анорексия, похудание, истощение подкожного жирового слоя и мышц, распространенные отеки, асцит, холелитиаз, увеличение печени, ахлоргидрия, диарея. Могут наблюдаться коричневые пятна пигментации на сухой, бледной, холодной коже; увеличение околоушных слюнных желез, анемия, гипертрофическая остеоартропатия, потеря либидо у мужчин, аменорея у женщин. Выраженность клинических проявлений зависит от степени тяжести трофологической недостаточности и определяет качество жизни пациентов. Поэтому важной задачей клинициста служит раннее выявление трофологической недостаточности у больных циррозом печени и проведение ее адекватной коррекции.
Лечение проводится с учетом всех механизмов развития трофологической недостаточности при циррозе печени и включает:
прекращение приема алкоголя;
обеспечение полноценного питания пациентов (особенно больных алкогольным циррозом печени);
заместительную терапию препаратами ферментов поджелудочной железы;
заместительную терапию витаминами;
энтеральное и парентеральное питание растворами белков при снижении синтетической функции печени.
Прекращение приема алкоголя не только благоприятно влияет на трофологический статус, но и позволяет замедлить прогрессирование цирротического процесса у больных алкогольным циррозом печени. Полноценное питание должно обеспечивать организм больного адекватными количествами основных питательных веществ (белков, жиров и углеводов), витаминов, микроэлементов и энергии. Общая энергетическая ценность пищи должна составлять не менее 2 000 ккал в сутки.
Изменения со стороны желчевыводящих путей как причина развития болей в животе при циррозе печени
При циррозе печени с повышенной частотой выявляется дискинезия желчевыводящих путей и холелитиаз, что связывают с нарушением коллоидных свойств желчи и регуляции моторики желчевыводящих путей. Соответственно, среди всех причин болей в животе при циррозе печени билиарная боль занимает весьма важное место. Билиарная боль может носить характер висцеральной или соматической, что, в общем, отражает механизм ее возникновения.
Висцеральная билиарная боль возникает в ответ на быстрое нарастание внутрипротокового давления и растяжение стенки желчного пузыря и желчевыводящих путей. При этом скорость нарастания внутрипросветного давления пропорциональна интенсивности боли.
Повышение внутрипротокового давления может сопровождаться рефлекторной тошнотой, рвотой, не приносящей облегчения, другими вегетативными реакциями. В своем классическом проявлении билиарная висцеральная боль носит характер печеночной, или желчной, колики. Между приступами болевые ощущения полностью отсутствуют. При осмотре пациента определяется неотчетливо локализованная болезненность в эпигастральной области и правом подреберье; может отмечаться нарастание уровня билирубина вследствие обструкции желчевыводящих путей.
Соматическая билиарная боль обусловлена вовлечением в воспалительный процесс брюшинного покрова желчевыводящих путей. При пальпации живота определяется локальная болезненность в правом подреберье, защитное напряжение мышц передней брюшной стенки, ограничение дыхательных движений при глубокой пальпации правого подреберья, симптомы раздражения брюшины. Как правило, развиваются лихорадка и лейкоцитоз в крови. В купировании и предупреждении приступов желчной колики и болей, связанных с дискинезией желчевыводящих путей, основное место принадлежит препаратам со спазмолитическим действием. В лечении острого воспалительного поражения желчевыводящих путей с вовлечением брюшины главная роль принадлежит хирургическому вмешательству.






